2019年8月21日,我院眼科研究所李志杰教授实验室在国际权威学术期刊《Mucosal Immunology》(JCR医学一区杂志,影响因子7.35)上发表了题为“Antibiotic-induced dysbiosis of gut microbiota impairs corneal development in postnatal mice by affecting CCR2 negative macrophage distribution”的研究成果。此项工作揭示了肠道菌群失调影响角膜发育过程的新机制。本研究由我院刘俊副研究员和再生医学专业的硕士研究生邬明娟作为共同第一作者完成。
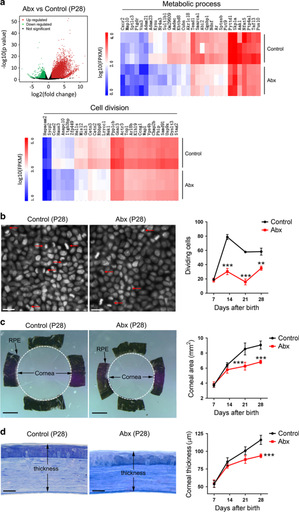
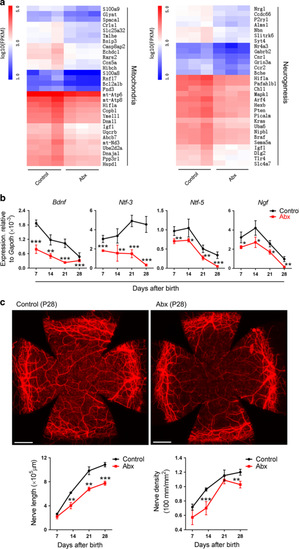
新生儿出生后的视力发育尚未完成,容易受到外部因素的影响,如营养的缺失、过度的用药和光线刺激都有可能引起异常的眼球生长和神经的变化,造成永久的视力损害。近年的研究表明肠道菌群作为人类的第二基因组与人类的发育和健康密切相关。新生儿对病原体易感性高,容易发生感染。临床数据显示超过半数的新生儿在出生后第一个月内会接受抗生素的治疗。这些抗生素的使用对新生儿肠道菌群和眼角膜发育的影响及其作用机制目前并不清楚。该研究发现连续两周的抗生素处理后新生小鼠的肠道菌群组成和多样性发生剧烈改变。与此同时,角膜的形态发育、角膜神经纤维和角膜缘血管网的形成过程明显受阻。这些效应可延续到成年期。然而,在早期通过粪菌移植和补充益生菌实施干预在很大程度上可显著逆转上述角膜发育进程的延迟。进一步的研究表明抗生素驱动的菌群失调主要通过抑制CCR2─巨噬细胞(而非CCR2+巨噬细胞)在发育角膜中的分布和募集以及减少多种特异性生长因子的产生来发挥关键性作用。该研究为了解眼角膜的发育过程、影响因素及其作用机制提供了新的数据,并为未来寻找新的防治措施来规避角膜发育缺陷提供了重要线索。
本研究以暨南大学基础医学院眼科研究所和再生医学教育部重点实验室为主要研究平台,并受到国家自然科学基金(资助号码:81470603, 81770962和81700808)、中国博士后基金(2017M622913)和广东省博士启动基金(2018A030310605)等项目的资助。
原文链接:https://www.nature.com/articles/s41385-019-0193-x

![{{siteInfoList.info[5]}}](/_upload/tpl/06/0d/1549/template1549/images/logo.png)
